双向电泳之样品的制备
一般性原则:
样品制备是双向电泳中最为关键的一步,这一步处理的好坏将直接影响2-DE 结果。目前并没有一个通用的制备方法,尽管处理方法是多种多样,但都遵循几个基本的原则:
1)尽可能的提高样品蛋白的溶解度,抽提最大量的总蛋白,减少蛋白质的损失;
2)减少对蛋白质的人为修饰;
3)破坏蛋白质与其他生物大分子的相互作用,并使蛋白质处于完全变性状态。
根据这一原则,样品制备需要四种主要的试剂:离液剂(chaotropes),主要包括尿素(Urea)和硫脲(thiourea);表面活性剂(sufactants),也称去垢剂,早期常使用NP-40、TritonX -100 等非离子去垢剂,近几年较多的改用如CHAPS 与Zwittergent 系列等双性离子去垢剂;还原剂(reducing agents ),最常用的是二硫苏糖醇(DTT),也有用二硫赤藓糖醇(DTE)以及磷酸三丁酯(TBP) 等。当然,也可以选择性的加入Tris-base,蛋白酶抑制剂( 如EDTA 、PMSF or Protease inhibitor c℃ktails )以及核酸酶。
样品的来源不同,其裂解的缓冲液也各不相同。通过不同试剂的合理组合,以达到对样品蛋白的最大抽提。在对样品蛋白质提取的过程中,必须考虑到去除影响蛋白质可溶性和2DE 重复性的物质,比如核酸、脂、多糖等大分子以及盐类小分子。大分子的存在会阻塞凝胶孔径,盐浓度过高会降低等电聚焦的电压,甚至会损坏IPG 胶条;这样都会造成2-DE 的失败。样品制备的失败很难通过后续工作的完善或改进获得补偿。
核酸的去除可采用超声或核酸酶处理,超声处理应控制好条件,并防止产生泡沫;而加入的外源核酸酶则会出现在最终的2D 胶上。脂类和多糖都可以通过超速离心除去。透析可以降低盐浓度,但时间太长;也可以采取凝胶过滤或沉淀/重悬法脱盐,但会造成蛋白质的部分损失。因此,处理方法必须根据不同的样品、所处的状态以及实验目的和要求来进行选择。
样品制备程序:
⒈培养细胞(culture cell)样品处理方法:
培养动物组织细胞由于没有细胞壁,因此可以将细胞收集下来,直接加入裂解缓冲液(Lysis buffer)抽提总蛋白。裂解缓冲液有多种配方,本实验室主要采用如下成份:
(A) 7M Urea,2M Thiourea,4%(w/v)CHAPS,40mM Tris-Base,40mM DTT,2% Pharmalyte pH 3-10.
其他常用的裂解缓冲液如下:
(B) 9.5M urea, 2%(w/v) CHAPS, 0.8%(w/v) Phamarlyte pH3 -10,1%(w/v) DTT and 5mM Pefabl℃ proteinase inhibitor;
(C) 加入0.3 -1% SDS 在95 ℃ 煮样品5mins ,冷却后加入至少5倍体积的(A)或(B)裂解液。
总蛋白抽提程序:
(1) 培养细胞的收集;
(2) 用磷酸缓冲液(PBS)洗细胞3 次(室温,1000g, 各2min);
(3) 将细胞分装到1.5ml Eppendof 管中,吸干残留的PBS;
(4) 加入裂解缓冲液(1.5x106 个细胞大约加入100µL 裂解液),在室温振荡1h,使其充分溶解;
(5) 4℃,40,000g,离心1h;
(6) 吸取上清并用Brandford 法定量蛋白,然后分装至Eppendof 管里保存在-78℃ 备用。
组织样品处理方法:
对大多数从动物或植物组织里提取总蛋白质而言,同样没有一种通用的程序。但遵循的原则基本相同。下面列出一种对植物树叶总蛋白的方法。
三氯醋酸-丙酮沉淀法(TCA/acetone precipitation)提取植物树叶总蛋白程序:
(1) 在液氮中研碎叶片;
(2) 悬浮于含10%三氯醋酸(TCA)和0.07%ß-巯基乙醇(可用DTT替代)的丙酮溶液在-20 ℃ 的冰浴;
(3) 让蛋白质沉淀过夜然后离心(4℃,40,000g, 1h),弃上清;
(4) 重悬沉淀浮于含0.07%β -巯基乙醇的冰预冷丙酮溶液里;
(5) 离心(4℃,40,000g, 1h)后真空干燥沉淀;
(6) 用(A)或(B)裂解液溶解沉淀,离心(4℃,40,000g, 1h)。
(7) Brandford 法定量蛋白,然后分装至Eppendof 管里保存在-78℃备用。
超速离心法:
(1)取材;
(2)用研钵在液氮冷冻条件下将样品研成粉末,每1g 样品加入0.5ml 裂解液,使用组织匀浆器匀浆30 s;
(3)组织悬液15℃,10 000×g 离心10 min;
(4)上清液4℃,150 000×g 超速离心45 min;
(5)小心避开上层漂浮的脂质层,吸取离心上清6℃ 40,000g 再次离心50 min;
(6)取离心上清。Bradford 法定量,分装后置–75℃保存。
文献报道较多的裂解液配方
Lysis buffer A
(9 M urea, 4% w/v CHAPS, 1% w/v DTT, 0.5% CA and a cocktail of protease inhibitors)
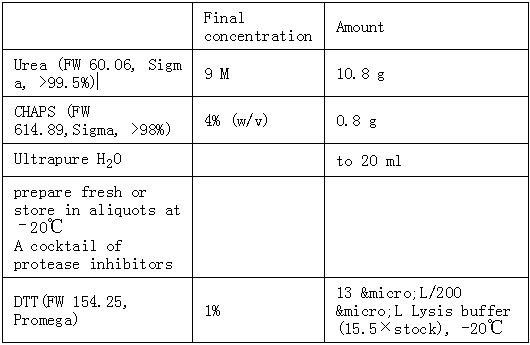
Lysis buffer B
(7 M urea, 2 M thiourea, 4% w/v CHAPS, 1% w/v DTT, 0.5% CA and a cocktail of protease inhibitors)
Lysis buffer C
40 mM Tris-base (pH 9.5) in ultrapure H2O
Lysis buffer D
(8 M urea, 4% CHAPS, 40 mM Tris(base), 40 ml)
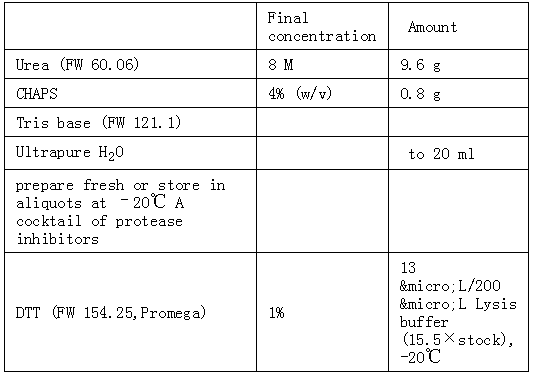
Lysis buffer E
(5 M urea, 2 M thiourea, 2% SB 3-10, 2% CHAPS, 1% w/v DTT, 0.5% CA and a cocktail of protease inhibitors)
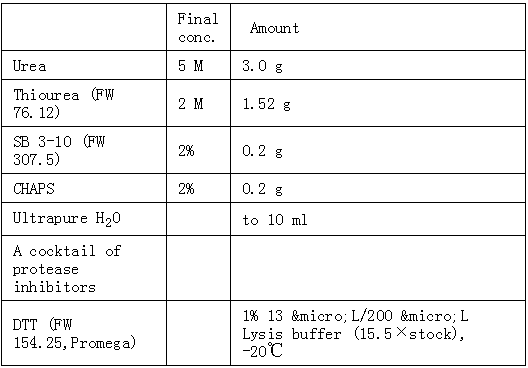
Lysis buffer F
100 µL SDS sample solution (1% w/v SDS, 0.375 M Tris-HCl, pH 8.8, 50 mM DTT,25% v/v glycerol
注:CA、蛋白酶抑制剂混合物和DTT在临用前加入。
广谱蛋白酶抑制剂混合物(如加tris 可不用此混合物)
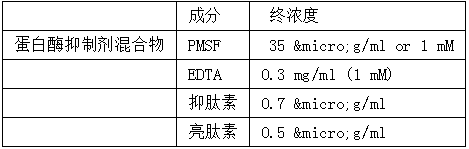
其中C-F 是分步法提取的4 种裂解液配方, C 适于提取水溶性蛋白,D是经典配方,E适于提取膜蛋白配方,F 适于提取难溶的沉淀蛋白。